2021年美国FDA批准的新药大盘点
2021年FDA共批准50款新药(不包括细胞疗法和疫苗),包括36个新分子实体和14个新生物制品,其中34%是突破性疗法,First in class超40%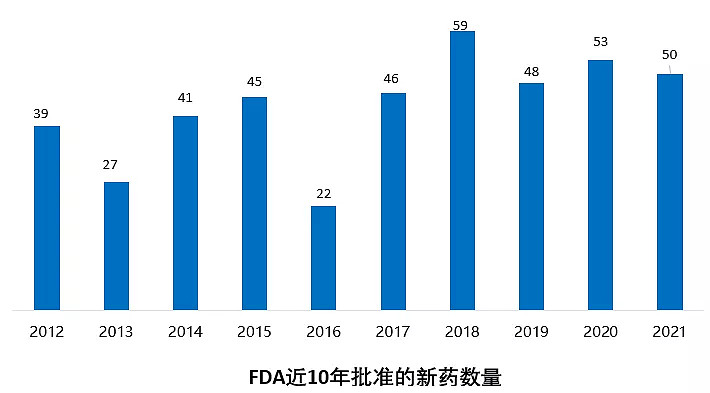
从疾病领域来看,2021年FDA批准的新药仍以肿瘤药居多,占比30%(15/50),其他占比较高的疾病领域还包括自身免疫性疾病(14%,7/50)、内分泌代谢(12%,6/50)、神经精神(10%,5/50)、遗传性疾病(10%,5/50)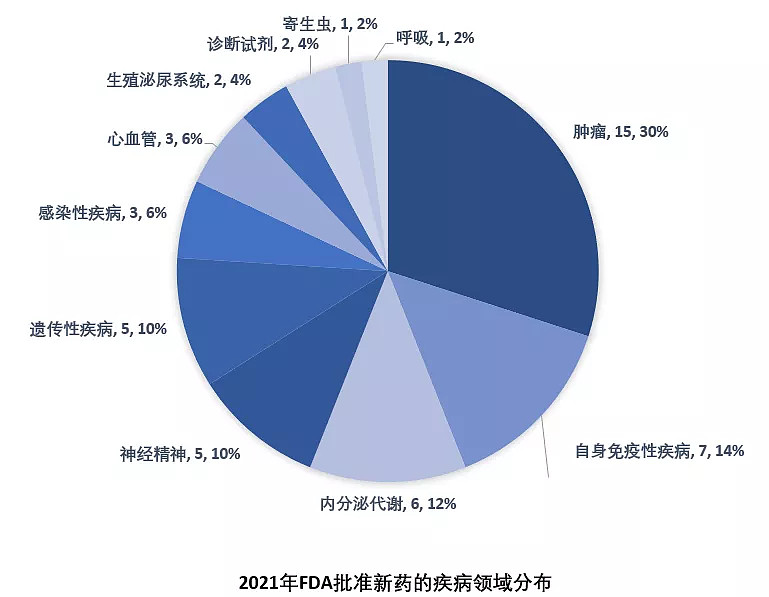
从审评方式上看,今年共有34个新药是以“优先审评”的方式获得FDA批准上市,其中包括27个新分子实体和7个新生物制品。有26个品种被FDA授予“孤儿药”资格,占所有获批新药的52%
2021年FDA获批的新药中,有21款(42%)属于First in class药物,有17款(34%)曾被FDA授予突破性疗法(BTD)资格,这两组数据也证明了今年批准新药的创新含量极高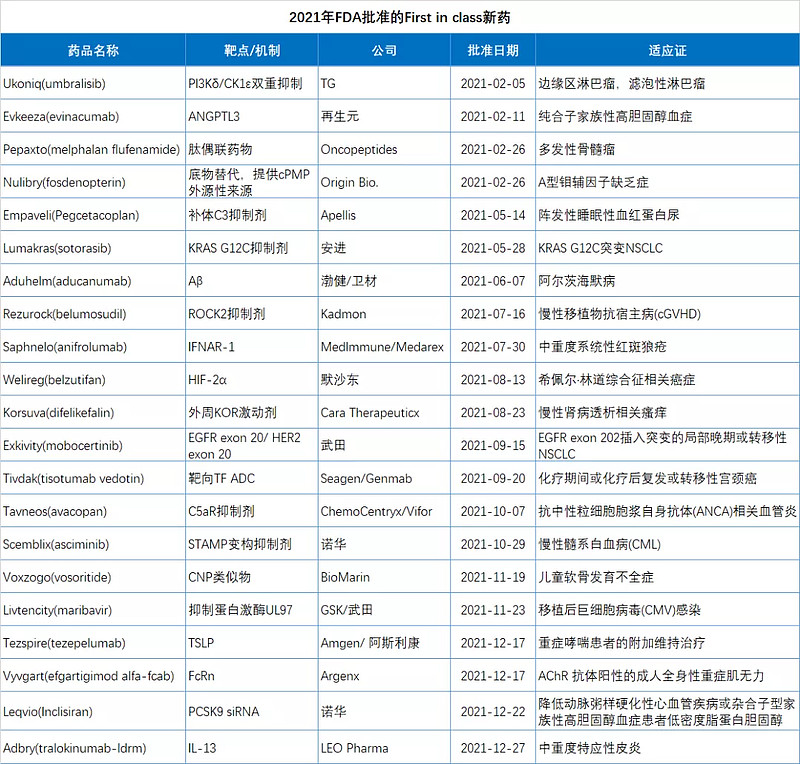
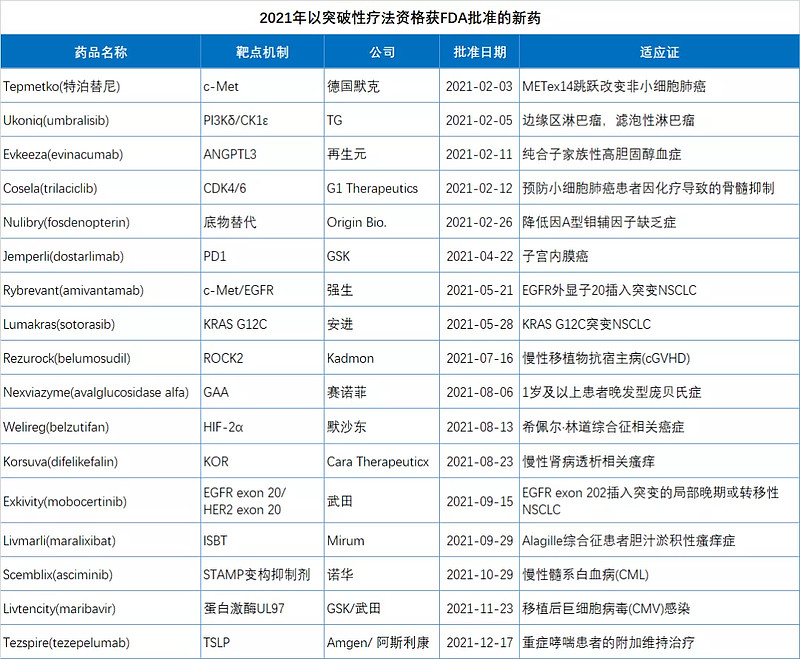
此外,FDA在2021年还批准了2款细胞疗法和5款疫苗,两款细胞疗法均来自BMS(百时美施贵宝),有两款疫苗来自辉瑞,其中就包括预防新冠肺炎的mRNA疫苗Comirnaty。
2021年FDA批准上市的细胞疗法和疫苗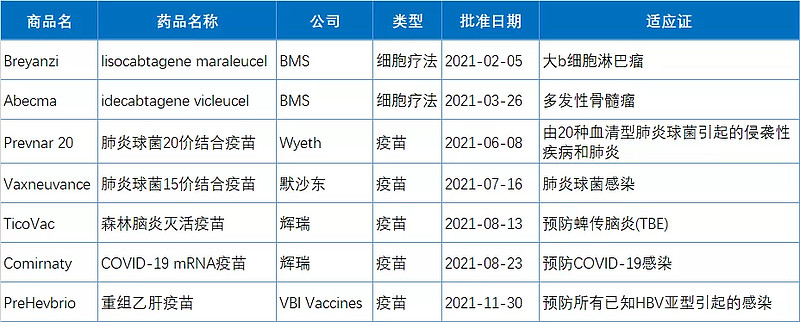
为应对新冠疫情,今年FDA对多款新冠治疗/预防药物授予了紧急使用授权(EUA),其中包括默沙东、辉瑞的口服小分子药,君实/礼来、GSK/Vir、阿斯利康等制药企业的新冠中和抗体以及Genentech的IL-6R单抗。
2021年FDA批准紧急授权使用的药物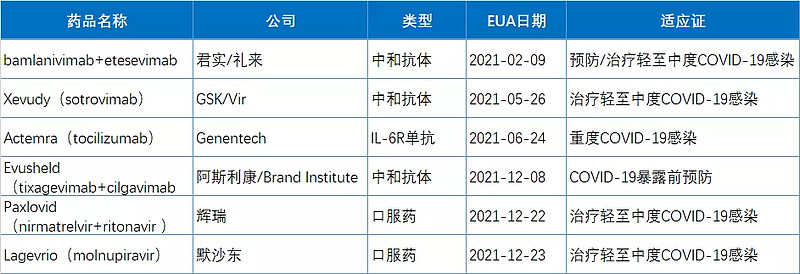
由于篇幅所限,本文对2021年批准的17个突破性疗法进行简单介绍。
NO.1 Tepmetko(特泊替尼)
适应症:治疗携带MET基因第14号外显子(MET ex14)跳跃突变的转移性非小细胞肺癌(NSCLC)成人患者,无论这些患者之前是否已接受过治疗。
MET ex14跳跃突变占NSCLC病例的3%~4%,这类侵袭性肺癌患者通常是老年人,预后较差。目前临床迫切需要能够产生持久抗肿瘤活性的靶向疗法以改善这种挑战性疾病患者的生活。
Tepmetko由德国默克自主研发,可抑制MET基因突变引起的致癌MET受体信号。该产品最早于2020年3月在日本获批上市,是全球首个获得监管部门批准用于治疗MET基因突变晚期NSCLC的口服MET抑制剂,同时也是FDA批准的首个也是唯一一个每日口服1次的MET抑制剂。
在中国,默克最早于2013年7月向NMPA递交临床申请,截止目前已在中国开展4项临床研究。
NO.2 Ukoniq(umbralisib)
适应症:用于治疗之前至少接受过一种基于抗CD20治疗方案的复发或难治性边缘区淋巴瘤(MZL)成人患者和之前至少接受过三线全身治疗的复发或难治性滤泡性淋巴瘤(FL)成人患者。
Umbralisib由TG公司开发,是首个也是唯一一个获批上市的每日口服1次的磷酸肌醇3激酶(PI3K ) δ和酪蛋白激酶1 (CK1) ε抑制剂。
MZL和FL适应症的加速获批是基于一项开放标签,多中心,双队列II期UNITY-NHL研究总缓解率(ORR)数据。研究结果表明,MZL患者的总缓解率(ORR)为49% ,完全缓解率(CR)为16%,中位缓解持续时间(DOR)尚未达到。FL患者ORR为43%,CR为3.4%,DOR为11.1个月。
NO.3 Evkeeza(evinacumab)
适应症:作为其他降脂药物的辅助疗法用于治疗成人和12岁以上儿科纯合子家族性高胆固醇血症(HoFH)。
Evkeeza由再生元开发,是FDA批准的首个靶向血管生成素样蛋白3(ANGPTL3)的药物。ANGPTL3是肝脏分泌的一种蛋白,主要在人和小鼠肝脏表达,在脂质代谢中发挥着关键作用,与脂代谢紊乱、冠心病与动脉粥样硬化、糖尿病、代谢综合征、肾病以及肝癌等疾病有关。
Evkeeza通过静脉注射给药,每月注射1次,给药剂量依体重换算(15mg/kg),因此每个人按照WAC价格的年治疗费用并不相同,平均大约为45万美元/年。再生元通过myRARE™项目期望能为符合条件的患者提供援助。在该项目下,商业保险覆盖范围内的符合条件患者,有机会接受免费治疗。
Evkeeza目前尚未在国内申报临床,国内开发ANGPTL3靶向药的企业有诺华和辉瑞。
NO.4 Cosela(trilaciclib)
适应症:预防扩散期小细胞肺癌成人患者因铂类/依托泊苷方案或拓扑替康方案化学治疗导致的骨髓抑制。
Trilaciclib由G1Therapeutics开发,是全球首个也是唯一一个化疗开始前预防性给药以保护骨髓和免疫系统功能的产品。
Trilaciclib是First-in-class的短效小分子CDK 4/6抑制剂,在化疗前预防性使用,可以将骨髓细胞短暂阻滞在细胞周期的G1期,显著减少化疗药对骨髓细胞的杀伤,保护骨髓细胞和免疫系统功能。
2020年8月,先声药业与G1公司达成独家许可协议,获得了trilaciclib在大中华地区所有适应症的开发和商业化权益,并将参与其在全球的临床试验。
据CDE网站公示,先声和G1 Therapeutics联合申报的trilaciclib的上市申请已获NMPA受理并被纳入了优先审评,适应症为在接受含铂类药物联合依托泊苷方案的广泛期小细胞肺癌(ES-SCLC)患者中预防性使用trilaciclib,以降低化疗引起的骨髓抑制的发生率。
NO.5 Nulibry(fosdenopterin)
适应症:用于降低因A型钼辅因子缺乏(MoCD)导致的死亡风险。
Nulibry由BridgeBio子公司Origin Biosciences开发,是FDA批准的首款治疗该疾病创新疗法。MoCD是一种罕见的、遗传代谢性疾病,通常发病于出生几日的婴儿,会导致顽固性癫痫发作、脑损伤和死亡。全球共不到150例患者受此疾病影响,患者中位生存时间为4年。
Fosdenopterin是一种底物替代疗法,提供了cPMP(环吡喃单磷酸)的外源性来源,cPMP可转化为钼嘌呤,而钼嘌呤又可转化为钼辅因子,以防止因钼辅因子缺乏而导致的亚硫酸盐氧化酶合成减少进而导致的毒亚硫酸盐的积累,从而缓解婴幼儿A型MoCD的中枢神经系统症状。
NO.6 Jemperli(dostarlimab)
适应症:治疗此前接受含铂化疗后疾病进展,且存在DNA错配修复缺陷(dMMR)的成人复发性或晚期子宫内膜癌。
Dostarlimab是FDA批准的第7款程序性死亡受体-1 (PD-1)阻断抗体,能够与PD-1受体结合,从而阻断其与PD-L1和PD-L2配体结合,抑制肿瘤免疫逃逸。Dostarlimab最初由AnaptysBio公司发现,2014年3月TESARO获得了在全球开发和商业化dostarlimab的权利,2018年12月GSK收购TESARO,将dostarlimab收入囊中。
今年8月17日,dostarlimab新适应症获FDA批准,用于治疗存在错配修复缺陷(dMMR)复发或晚期实体瘤患者。
NO.7 Rybrevant(amivantamab)
适应症:治疗铂类化疗后进展的EGFR外显子20插入突变的转移性非小细胞肺癌(NSCLC)患者。
Rybrevant由强生开发,是一款EGFR/c-Met双抗,于5月21日凭I期临床数据获FDA加速批准上市,是FDA批准的首款针对EGFR外显子20插入突变药物。
Rybrevant在中国也于2020年9月获得了CDE授予的突破性疗法资格。目前国内开发EGFR/c-Met双抗药物的公司有岸迈生物、贝达药业、嘉和生物。
NO.8 Lumakras(sotorasib)
适应症:治疗既往至少接受过一次系统治疗的携带KRAS G12C突变局部晚期或转移性非小细胞肺癌(NSCLC)患者。
Lumakras由安进开发,是全球首个获得批准的靶向KRAS突变的肿瘤治疗药物。
Sotorasib已于今年1月28日被CDE纳入突破性疗法,国内已申报临床的KRAS G12C抑制剂的企业除了安进外,还包括贝达药业、北京加科思、益方生物、劲方药业、勤浩医药、诺华。
NO.9 Rezurock (belumosudil)
适应症:治疗12岁以上的慢性移植物抗宿主病(cGVHD)患者,这些患者已经接受过两种前期全身性治疗。
造血干细胞移植是治疗血液或骨髓癌症的常见手段。然而,在cGVHD患者中,移植的免疫细胞会攻击宿主的健康细胞,从而带来一系列严重的副作用。据估计,大约有30%-70%接受造血干细胞移植的患者会出现cGVHD症状,包括炎症反应和多器官组织纤维化。
Belumosudil是first-in-class口服选择性 ROCK2抑制剂,ROCK2是一种调节免疫应答和纤维化途径的信号通路。belumosudil可通过抑制ROCK2信号通路,下调促炎性Th17细胞、增加调节性T(Treg)细胞,重新平衡免疫应答,治疗免疫功能障碍。
2019年11月烨辉医药与Kadmon达成一项许可协议,负责belumosudil在中国大陆地区cGVHD适应症的开发和商业化。该产品已于2020年11月被CDE纳入突破性疗法。
NO.10 Nexviazyme(avalglucosidase alfa)
适应症:1岁及以上患者晚发型庞贝氏症。
庞贝病是一种进行性、使人衰弱的肌肉疾病,由溶酶体中的酸性α-葡萄糖苷酶(GAA)的遗传缺陷或功能障碍引起。GAA会导致全身肌肉细胞中糖原的积累,从而导致不同肌肉不可逆的损伤,包括支持呼吸功能的膈肌和影响人体活动、功能耐力和呼吸的骨骼肌。
Nexviazyme由赛诺菲开发,是一款酶替代疗法(ERT)。它能够特异性靶向细胞摄取的关键途径甘露糖-6-磷酸(M6P)受体。与标准治疗α-葡萄糖苷酶相比,Nexviazyme的M6P含量增加约15倍,从而帮助改善细胞对酶的摄取并增强目标糖原清除。
据了解,Nexviazyme针对儿童患者的年治疗费用约为330,000 美元,成人患者约为758,000美元。
NO.11 Welireg(belzutifan)
适应症:治疗希佩尔·林道综合征 ( von Hippel-Lindau,VHL) 疾病相关癌症,包括:肾细胞癌(RCC)、中枢神经系统(CNS)血管母细胞瘤或胰腺神经内分泌肿瘤(pNET),这些患者不需要立即手术。
VHL是一种罕见的遗传性疾病,每3.6万人中就有1人患病,在美国估计有1万人患VHL。VHL患者不仅有罹患良性血管肿瘤的风险,也有罹患某些癌症的风险,包括肾细胞癌。
Welireg是FDA批准的首个HIF-2α抑制剂疗法。通过抑制HIF-2α,Welireg可降低与细胞增殖、血管生成和肿瘤生长相关的HIF-2α靶基因的转录和表达。
默沙东于今年2月在国内申报belzutifan的临床申请,目前处于I期临床阶段。
NO.12 Korsuva(difelikefalin)
适应症:接受血液透析(HD)成人慢性肾病相关中重度瘙痒症(CKD-aP)。
CKD-aP是一种顽固的全身性瘙痒症,在接受透析的慢性肾病患者中具有较高的发生频率和强度,在未接受透析的III-V期CKD患者中也有报道。目前使用的止痒方案如抗组胺药和皮质类固醇无法提供持续、充分的缓解。中重度慢性瘙痒反复发作严重降低患者生活质量,并且可导致抑郁症。
Korsuva由Cara Therapeutics和Vifor Pharma联合开发,是一款first in class高选择性k阿片受体(KOR)完全激动剂,能够抑制产生瘙痒的外周神经元的活性,并且对其他受体(包括mu或delta阿片类受体)、离子通道或转运体无显著活性。
另外,不同于小分子KOR激动剂,Korsuva是一款小型合成肽,主要激活外周神经元(PNS)和免疫细胞表达的KORs。是FDA批准的首个也是唯一一个治疗此类患者的疗法。
NO.13 Exkivity(mobocertinib)
适应症:接受含铂化疗治疗中或治疗后疾病出现进展的携带EGFR外显子20插入突变的局部晚期或转移性非小细胞肺癌(NSCLC)患者。
Exkivity由武田开发,是一种专门设计用于选择性靶向EGFR外显子20插入突变的强效口服小分子酪氨酸激酶抑制剂。同时也是美国FDA批准的首款专门为携带EGFR外显子20插入突变的NSCLC患者设计的口服疗法。
在国内,mobocertinib已于2020年10月被CDE纳入突破性疗法。今年5月,其上市申请被纳入优先审评。
NO.14 Livmarli(maralixibat)
适应症:1岁及以上Alagille综合征(ALGS)患者的胆汁淤积性瘙痒。
Alagille综合征 (ALGS) 是一种罕见的遗传性疾病,因患儿胆管异常狭窄、畸形和数量减少导致胆汁在肝脏中积聚,最终导致肝病进展。ALGS肝损伤引起的体征和症状包括黄疸、黄疣和瘙痒症。其中,瘙痒症是所有慢性肝病中最严重的,并且大多数儿童3岁就会出现此症状。据估计,每30000个人中就有一人患ALGS。
Livmarli是一种每日口服1次的回肠胆汁酸转运体(IBAT)抑制剂,可通过抑制IBAT的再摄取改变胆汁酸的流向,阻断胆汁酸在肝脏的再循环,增加粪便胆汁酸排泄来防止胆汁酸在肝脏的积聚。Livmarli是FDA批准的首个也是唯一一个治疗这种罕见肝病的药物。
NO.15 Scemblix(asciminib)
适应症:加速审批,用于既往接受至少两种TKI治疗的费城染色体阳性CML慢性期(Ph+ CML-CP)成人患者,并完全获批用于T315I突变型Ph+ CML-CP成人患者。
20年前TKI的上市彻底改变了CML的治疗方法。然而,仍有许多患者对至少两种可用的疗法不能充分缓解。一项分析结果显示,接受过两种TKI治疗的CML患者中,约55%报告对先前的治疗不耐受。此外,一项二线治疗的汇总分析显示,高达70%的患者在随访两年内无法实现主要分子学缓解(MMR)。而发生T315I突变的患者对大多数可用TKI耐药,疾病进展风险显著增加。
Asciminib是一种专门针对ABL肉豆蔻酰口袋 (STAMP) 的药物。作为STAMP 抑制剂,asciminib与BCR-ABL1结合的位点与常见TKI不同,可能有助于解决CML后线治疗中TKI耐药和不耐受问题。
FDA此项批准是基于III期ASCEMBL试验和I期试验(NCT02081378)结果。ASCEMBL试验结果显示,治疗24周,asciminib vs 博舒替尼的MMR比率为25% vs 13%。因不良事件导致的停药率为7% vs 25%。
在国内,Asciminib 目前处于III期临床阶段。
NO.16 Livtencity(maribavir)
适应症:接受造血干细胞移植(HSCT)或实体器官移植(SOT)后成人或12岁以上儿童患者的难治性巨细胞病毒(CMV)感染。这些患者对已有针对CMV的抗病毒疗法不产生应答。
CMV是一种能感染人类的β疱疹病毒,是移植患者最常发生的感染之一,CMV在实体器官移植患者中的发生率约为16-56%,在造血干细胞移植患者中的发生率约为30-70%。目前的获批疗法不但具有严重的毒副作用,并且已产生耐药。
Livtencity通过抑制CMV病毒的pUL97蛋白激酶,阻断病毒的复制,与已有疗法相比具有更高的安全性。这是针对该患者群体的首款获批疗法。
NO.17 Tezspire(tezepelumab)
适应症:12岁及以上重症哮喘儿童和成人患者的附加维持治疗
Tezspire由阿斯利康和安进联合开发,是一款first in class生物制剂,通过阻断TSLP阻止免疫细胞释放促炎细胞因子,从而预防哮喘发作和改善哮喘控制。
目前治疗哮喘的生物制品只针对T2炎症,tezepelumab则具有不同的作用机制,能够阻断多条炎症信号通路上游的TSLP,在级联的顶端起作用,从源头上抑制炎症,从而治疗广泛的严重哮喘患者群体。
在国内,tezepelumab已处于III期临床阶段。开发TSLP靶向药的企业包括康诺亚、和铂医药、恒瑞医药。
附表: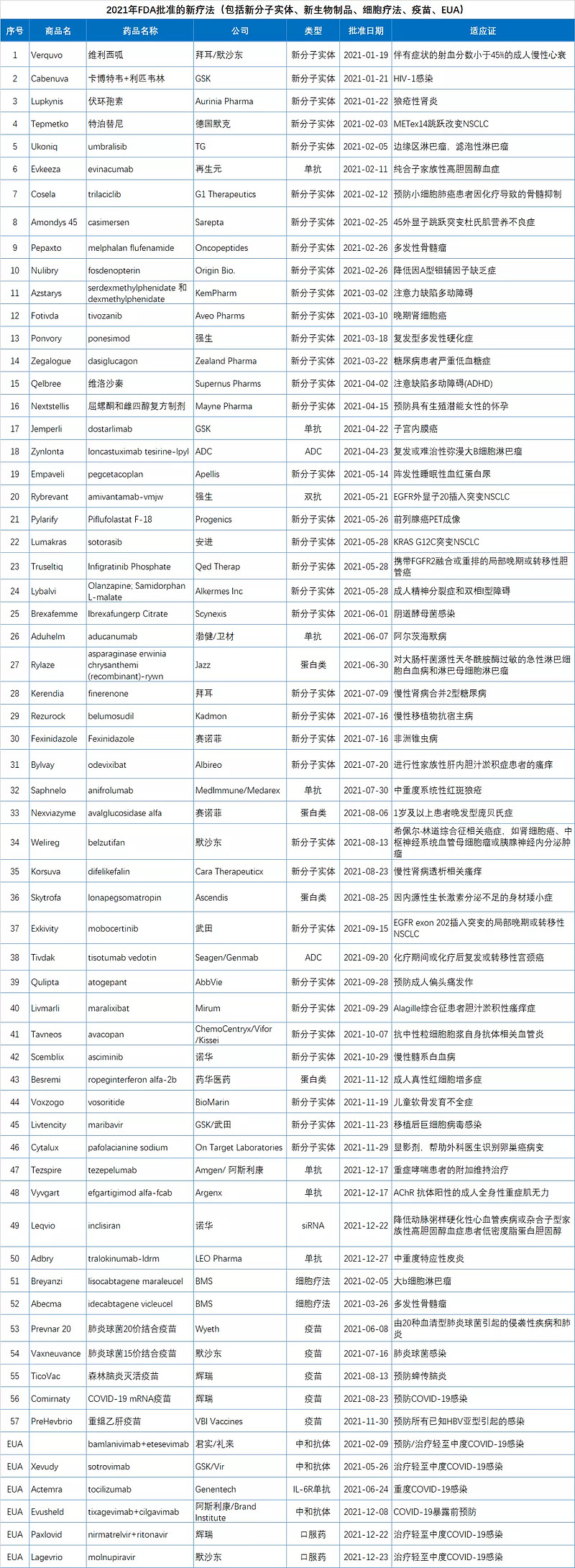
转载自:医药魔方 链接:https://xueqiu.com/8965749698/207431655