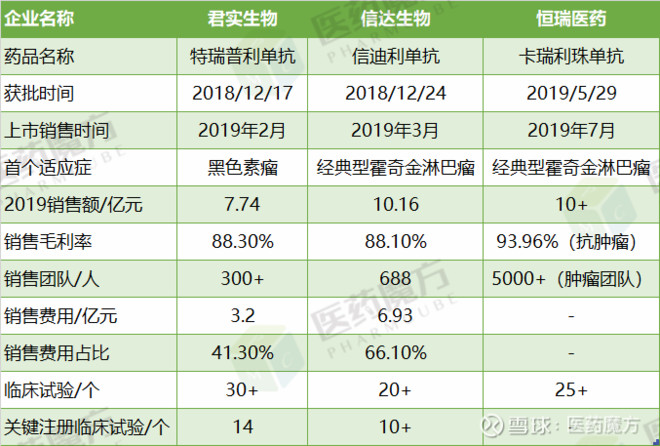
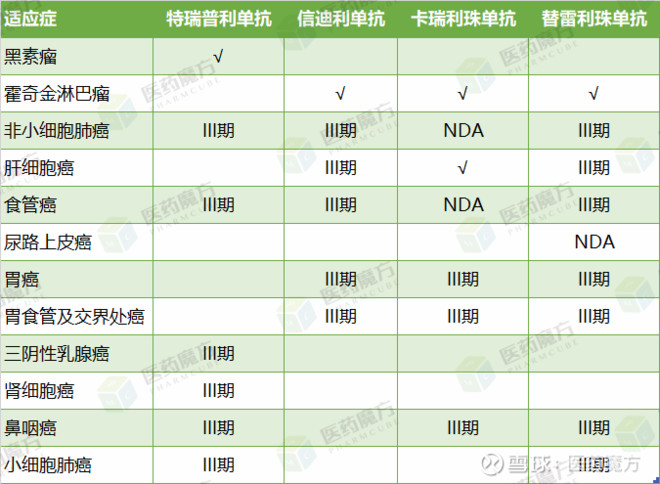
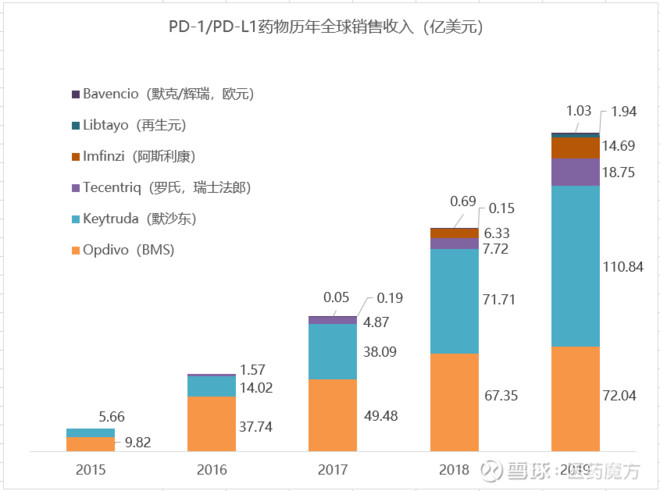
国内已上市的八款PD-1/PD-L1用药信息大盘点

在2019年的最后一个月,国内首款PD-L1免疫抑制剂Durvalumab(度伐利尤单抗,英飞凡)注射液获批上市;
紧接着,百济神州12月28日宣布,其抗PD-1抗体药物百泽安批准用于治疗至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤(R/R cHL)患者,这也标志着第4款国产PD-1终于获批;
而在2月13日,国内小细胞肺癌患者也终于迎来了首款PD-L1免疫检查点抑制剂。
至此,国内已有8款免疫检查点抑制剂上市,包括4款国产PD-1,2款进口PD-1和2款进口的PD-L1。中国的患者终于迎来了真正的免疫治疗元年!